Wissenschaft
COVID-19-Behandlung: Die klinische Entdeckungsstudie hat Schwierigkeiten, sich durchzusetzen
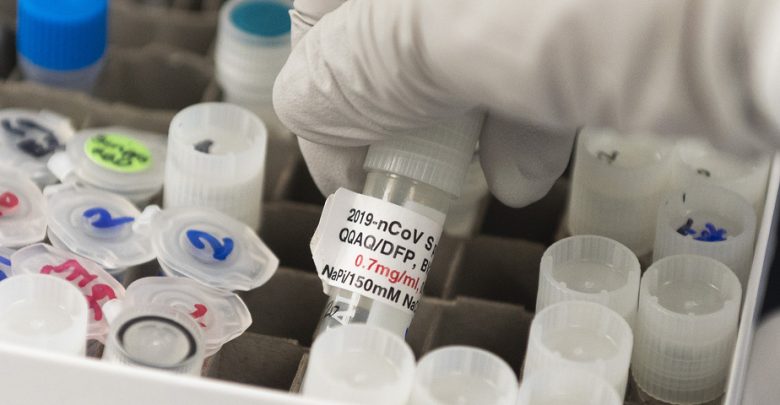
(Paris) Ende März mit großer Begeisterung gestartet, in der Hoffnung, eine Behandlung gegen COVID zu finden – 19 Die klinische Studie Discovery hat aufgrund der Eislauf-Zusammenarbeit in Europa und der Wirksamkeit, die bei den vier getesteten Arzneimitteln wahrscheinlich geringer ist als erwartet, noch keine Ergebnisse erbracht.
Amélie BAUBEAU
France Media Agency
Wenn eine klinische Studie durchgeführt wird, trifft sich regelmäßig ein Ausschuss externer Experten, das so genannte Data Safety Monitoring Board (DSMB), um die Daten zu analysieren und die Forscher zu beraten. Am Montag wiedervereinigt, urteilte derjenige, der Discovery folgt, dass es notwendig sei, die Studie fortzusetzen und weiterhin neue Patienten einzubeziehen, da zu diesem Zeitpunkt keine überzeugenden Ergebnisse vorliegen.
„Sie sagten uns, dass wir weitermachen sollten“, sagte Prof. Yazdan Yazdanpanah, einer der Forscher, die das Projekt am französischen Forschungsinstitut Inserm beaufsichtigten, gegenüber AFP.
Am Dienstag kam das unabhängige Komitee, das Daten aus Solidarität analysierte, einem großen Aufsatz der Weltgesundheitsorganisation (WHO), der Discovery enthält, zu den gleichen Ergebnissen, fügte er hinzu.
Am 4. Mai hatte der Präsident der Republik, Emmanuel Macron, jedoch angegeben, dass am Donnerstag „Ergebnisse“ erwartet würden. Er sprach von „einem wichtigen Schritt“, während er anerkannte, dass es im Moment „nichts aussagekräftiges gibt“.
Diese enttäuschte Erwartung ist nicht die erste für Discovery. Als dieser ehrgeizige Test am 19 März gestartet wurde, wurden die ersten Antworten in wenigen Wochen erwartet.
Dann hatte Professor Florence Ader, die es pilotierte, gewarnt, dass wir „mindestens Ende April“ auf die „ersten Trends“ warten müssten. Wieder ein verpasster Termin.
Der Kern des Problems ist die zu geringe Anzahl eingeschlossener Patienten: Im Moment werden 750 Patienten in diese Studie eingeschlossen, fast nur in Frankreich, als das Ziel darin bestand, in Europa zu rekrutieren 2020, einschließlich mindestens
in Frankreich.
Bei den vier bewerteten Behandlungen handelt es sich nicht um Moleküle, die speziell auf das neue Coronavirus abzielen, sondern um bereits vorhandene Medikamente, die „neu positioniert“ wurden. Wir gehen davon aus, dass sie eine „teilweise“ Wirksamkeit haben werden, erklärte Professor Ader 6. Mai während einer Anhörung durch den Senat.
„Je mehr die Moleküle teilweise wirksam sind, desto mehr Patienten brauchen wir in den Studien“, um zuverlässig feststellen zu können, ob sie einen echten Nutzen bringen, fügte sie hinzu.
„Trägermoleküle“
Die Methodiker der Discovery-Studie errechneten daher, dass „mindestens Patienten pro Arm erforderlich wären“) durch getestete Behandlung: das antivirale Remdesivir, die Kombination Lopinavir / Ritonavir (Kaletra), eine Kombination dieser antiretroviralen Mittel mit Interferon Beta und schließlich Hydroxychloroquin, abgeleitet von dem Antimalaria-Chloroquin. Plus eine fünfte Gruppe von Patienten, die „Standardversorgung“ erhalten, der Maßstab für die Beurteilung des Nutzens anderer Behandlungen.
„Dies sind keine Wundermoleküle, sondern Unterstützungsmoleküle, die, wenn sie zur richtigen Zeit und für die richtige Population verschrieben werden, nützlich sein können“, glaubt Professor Yazdanpanah, der das REACTing-Netzwerk koordiniert. ein Forschungskonsortium zu neu auftretenden Infektionskrankheiten.
Die DSMB, die „Anfang Juni“ erneut zusammentreten wird, hätte empfehlen können, die Studie abzubrechen, wenn sie „ein Problem für die Patientensicherheit“ gesehen hätten oder „wenn sie das sogar in gedacht hätten“ einschließlich 10 00 0 Leute, wir würden keinen Unterschied sehen ”.
Dort „sind sie der Ansicht, dass es kein Toxizitätsproblem gibt, dass sie keine größere Wirksamkeit sehen, aber dass sie durch Einbeziehung (mehr Patienten, Anmerkung des Herausgebers) vielleicht das „Wir können versuchen, Effizienz zu zeigen“, sagt der Spezialist für Infektionskrankheiten.
Um eine Chance zu geben, wird es jedoch dringend erforderlich, dass andere europäische Länder Patienten einbeziehen, während die Epidemie nachlässt und dass „die Einschlussrate in die Studie in Frankreich erheblich langsamer geworden ist“. nach Professor Ader.
Zunächst hatten mindestens sieben Länder, darunter das Vereinigte Königreich, Deutschland, Spanien oder Belgien, ihre Teilnahme angekündigt. Derzeit wurde jedoch nur „ein Patient“ außerhalb Frankreichs in Luxemburg eingeschlossen, erkannte der Forscher an.
“Wir schaffen es immer noch, 00 bei 15 Patienten pro Woche in Frankreich. Die Idee ist, dass wir dasselbe in anderen Ländern tun können „, bemerkt Yazdan Yazdanpanah, der versichert, dass Österreich“ nächste Woche „beginnen könnte, gefolgt von Deutschland, wo“ einige Formalitäten zu erledigen sind “ einstellen „.
Die Forscher verloren mehr Zeit als erwartet, „um die Regulierungsmanagementkreise von einem Land in ein anderes zu verstehen“, während in Frankreich die Gestaltung des Protokolls und die Genehmigungen in einem durchgeführt wurden Rekordzeit, bedauerte Florence Ader vor den Senatoren.
Professor Yazdanpanah bedauerte auch den 1. er Mai, a Europäisches „Scheitern“ der Forschung.
Derzeit laufen Gespräche mit der Europäischen Kommission, um die Regulierung klinischer Studien zu harmonisieren und eine nachhaltigere Finanzierung sicherzustellen, erklärt er.
Die mühsame Implementierung von Discovery wird „den Aufbau einer europäischen Plattform für klinische Studien“ vorangetrieben haben, in der Hoffnung, dass diese beim Testen der Discovery vorhanden sein wird „Moleküle der zweiten Generation“, die speziell für das neue Coronavirus entwickelt wurden.
